近年来,婴幼儿可食用益生菌成为越来越受欢迎的话题。研究表明肠道菌群对婴幼儿的影响较为突出。一方面,婴幼儿期是肠道菌群建立和发展的关键时期,此时菌群处于不稳定状态,容易受到各种因素的影响;另一方面,婴幼儿处于生理功能发育成熟的重要阶段,肠道菌群的良性建立对婴幼儿后期身体健康将产生长远的影响。
01、部分婴幼儿益生菌最新研究
随着母乳活性免疫成分、肠道菌群与婴幼儿健康关系的研究不断深入,尤其研究发现母乳中含有活的微生物,表明生命早期的微生物可能会对婴幼儿健康有着重要的意义,提示婴幼儿食品用益生菌的研究应被受到更广泛的关注。以下主要对鼠李糖乳酪杆菌HN001、罗伊氏粘液乳杆菌DSM17938和长双歧杆菌长亚种BB5363种菌种的研究情况进行介绍。
1.鼠李糖乳酪杆菌HN001
西安交通大学刘鑫、西安大兴医院田甜、汤臣倍健张旭光合作在《Gut Microbes》发表最新一项随机双盲安慰剂对照试验,评估补充膳食纤维或益生菌对功能性便秘症状的影响,并确定相关肠道微生物群的调节作用。该研究纳入250名功能性便秘患者,干预措施:A:葡聚糖;B:洋车前子;C:麦麸+洋车前草壳;D:动物双歧杆菌乳亚种HN019 +鼠李糖乳杆菌HN001;安慰剂:麦芽糊精。在第0、2和4周时,使用16S rRNA测序来评估肠道微生物群。排便频率(BMF)、布里斯托大便量表评分(BSS)和排便紧张程度(DDS)均无组间影响,而BSS在A组至D组平均增加0.95-1.05(P<0.05),而安慰剂组无显著变化(P=0.170),在第4周BSS的变化与安慰剂组相比同样显示出更佳的效果。D组患者血浆5-羟色胺含量明显降低。在第2周和第4周,A组的双歧杆菌丰度高于安慰剂。B组和C组厌氧菌呈上升趋势,与BMF升高有关。随机森林模型确定了预测干预应答者的特定基线微生物属组。研究表明膳食纤维或益生菌可以缓解硬便,肠道菌群的干预特异性改变与便秘缓解有关。基线肠道菌群可能倾向于干预反应[1]。
2.罗伊氏粘液乳杆菌DSM17938
《Gut Microbes》上发表的一项随机对照试验,研究了补充益生菌对SARS-CoV-2感染和COVID-19疫苗接种后抗SARS-CoV-2特异性抗体反应的影响。在这项随机、三盲、安慰剂对照、平行设计的干预研究中,159名健康成年人被随机分配到两个研究组,这些成年人之前没有感染过SARS-CoV-2或没有接种过COVID-19疫苗,也没有任何已知的严重COVID-19危险因素。积极治疗组每天两次食用含有至少1 × 108CFU的罗伊氏粘液乳杆菌DSM 17938 + 10μg维生素D3的益生菌产品,持续6个月;安慰剂组服用的是含有10 μg维生素D3的相同药片。从基线、3个月后和6个月后收集的血液样本中分析抗SARS-CoV-2特异性抗体和病毒中和抗体滴度。在意向治疗(ITT)分析中,积极治疗组(n = 6)的SARS-CoV-2感染者抗spike IgG及抗RBD IgG水平高于安慰剂组(n = 6)。考虑到完全接种了基于mRNA的COVID-19疫苗的个体,接种28天后,积极治疗组(n = 10)的血清抗RBD IgA水平明显高于安慰剂组(n = 7)。补充特定益生菌可能通过增强IgA反应来提高基于mRNA的COVID-19疫苗的长期疗效[2]。
3. 长双歧杆菌长亚种BB536
一项在日本进行的随机、双盲、安慰剂对照、平行组优势试验,80名诊断为慢性便秘的老年人被随机分配(1:1)接受益生菌(长梭菌BB536, 5 × 1010 CFU,n = 39)或安慰剂(n = 41),每天一次,持续4周。使用便秘评分系统评估便秘的严重程度。主要终点是两组在第4周便秘评分系统总分与基线变化的差异。共有79例患者(平均年龄77.9岁)完成了研究,其中BB536组38例,安慰剂组41例。主要终点无统计学意义(P = 0.074),但有显著改善,而安慰剂组无显著变化。在第4周,两组在大便频率和排便失败亚量表上的变化与基线相比有显著差异和趋势差异。几乎没有观察到与益生菌相关的不良事件。虽然主要终点无统计学意义,但补充益生菌可以显著改善肠道蠕动。这些结果表明,补充长柄双歧杆菌BB536对改善老年人慢性便秘是安全且部分有效的[3]。
02、可用于婴幼儿食品的菌种盘点
2022年8月25日,国家卫健委发布了关于《可用于婴幼儿食品的菌种名单》更新的公告,公告称,根据《中华人民共和国食品安全法》及其实施条例有关规定,为进一步规范《可用于婴幼儿食品的菌种名单》管理,审评机构组织专家对菌种名单进行了更新。
根据公告,《可用于婴幼儿食品的菌种名单》如下:
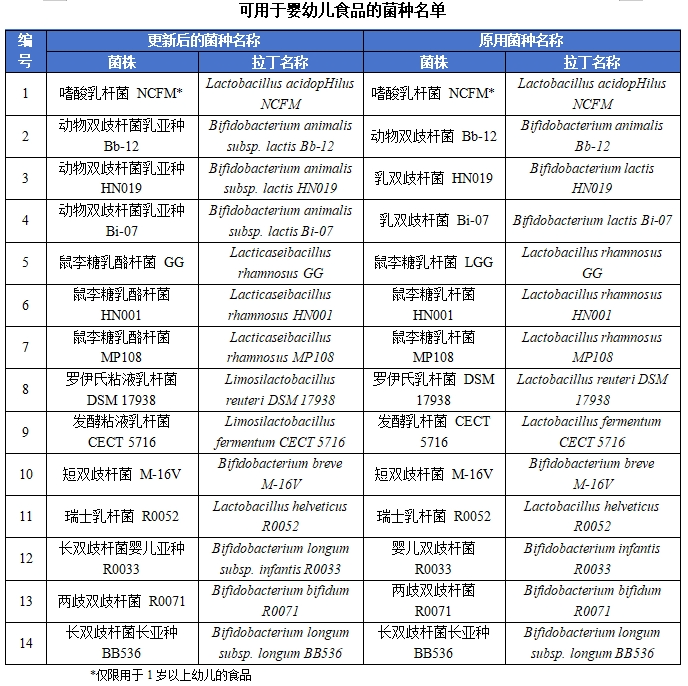
嗜酸乳杆菌 NCFM*:嗜酸乳杆菌NCFM(Lactobacillus acidophilus NCFM)属于乳杆菌科,乳杆菌属,能分解糖类生成L-乳酸,为上世纪70年代早期从北卡罗来纳州立大学从人体粪便中分离出来的菌株。
嗜酸乳杆菌NCFM已列入美国一般公认安全(GRAS)名单,被用于多种食品中,包括婴幼儿配方食品;已入欧洲食品安全局资格认定(QPS)名单的推荐生物制剂列表中,并列入国际乳品联合会公报(Bulletin of the IDF 455/2012)的“在发酵食品中有技术必要性的微生物品种目录”。国外开展的多项临床研究证明,该菌株用于1岁以下婴儿具有较好的食用安全性。2011年原中国卫生部(现中华人民共和国国家卫生健康委员会)已将嗜酸乳杆菌NCFM列入《可用于婴幼儿食品的菌种名单》,限定其仅用于1岁以上幼儿食品。2021年2月18日国家食品安全风险评估中心发布《新食品原料嗜酸乳杆菌NCFM公开征求意见》本次申请扩大用于1岁以下婴儿食品。
动物双歧杆菌乳亚种 Bb-12:动物双歧杆菌乳亚种Bb-12(Bifidobacterium animalis subsp. lactis Bb-12),双歧杆菌是从母乳喂养的婴儿粪便中发现并分离出来的,是人体肠道固有菌群的常见组成部分,其中动物双歧杆菌乳亚种Bb-12源自科汉森收集的乳品发酵剂,被鉴定为动物双歧杆菌乳双歧亚种,在食品中具有较高的稳定性。
动物双歧杆菌乳亚种Bb-12菌株已获得欧洲食品安全局(EFSA)授予的“安全资格认定”(QPS,Qualified Presumption of Safety),美国食品药品监督管理局 (FDA, Food And Drug Administration) 也已将动物双歧杆菌乳亚种Bb-12菌株列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)。国家发改委公众营养与发展中心组织专家对其进行论证认为,动物双歧杆菌乳亚种Bb-12可促进肠道菌群平衡,并提高人体免疫力。2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。
动物双歧杆菌乳亚种 HN019:动物双歧杆菌乳亚种HN019(Bifidobacterium animalis subsp. lactis HN019)菌株是一种革兰氏阳性、厌氧杆状细菌,最初是从新西兰酸奶源分离出来的,其凭借体外耐胆汁和低PH环境的能力,被认为是最具潜力的益生菌。动物双歧杆菌乳亚种HN019的食品,被日本政府的消费者厅批准为含健康声称的食品,是日本首个允许食品生产商在产品上进行健康声称的乳双歧杆菌菌株。
乳双歧杆菌HN019获得了欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、美国食品药品监督管理局 (FDA, Food And Drug Administration) 也已将动物双歧杆菌乳亚种HN019菌株列为“一般公认安全物质”(GRAS, Generally Recognized as Safe),2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。
动物双歧杆菌乳亚种 Bi-07:动物双歧杆菌乳亚种Bi-07(Bifidobacterium animalis subsp. lactis Bi-07)来源于人体,能在牛奶中生长。革兰氏阳性、厌氧、不产芽孢的多型性杆菌,体外研究表明显示动物双歧杆菌乳亚种Bi-07拥有良好的胃肠道表现,动物双歧杆菌乳亚种Bi-07可以抵抗低PH的条件(在PH3含1%胃蛋白酶的盐酸溶液中37℃培养1小时,存活率达90%以上),并可以在胆盐存在的环境下存活(含0.3胆盐的培养基培养,存活率大于90%)。
动物双歧杆菌乳亚种Bi-07被列入欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”、美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe),2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。
鼠李糖乳酪杆菌 GG:鼠李糖乳酪杆菌GG(Lacticaseibacillus rhamnosus GG)是从健康人体肠道中分离得来,自1990年以来鼠李糖乳酪杆菌GG菌株在全世界范围内被用作食品原料和膳食补充剂的成分。已有超过250篇临床研究文献对其进行了论述,其中涵盖新生儿、早产儿、儿童、孕妇、成年人、老年人等人群的不同健康领域。经过上千次科学研究证实鼠李糖乳酪杆菌GG能平衡肠道菌群,改善肠道健康、增强肠粘膜屏障、预防和治疗腹泻等作用。
鼠李糖乳酪杆菌GG已获得欧洲食品安全局(EFSA)授予的“安全资格认定”(QPS,Qualified Presumption of Safety) ,被美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe),2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。
鼠李糖乳酪杆菌 HN001:鼠李糖乳酪杆菌HN001(Lacticaseibacillus rhamnosus HN001)最初从新西兰生产的切达干酪中分离出来,它存在于乳制品中并拥有悠久的食用历史。在新西兰乳业研究所筛选出的200个菌株中,鼠李糖乳酪杆菌HN001被鉴定为潜在的益生菌菌株,用于进一步的动物和人体研究。该菌株被保藏于澳大利亚政府分析实验室(AGAL)。
鼠李糖乳酪杆菌HN001已列入欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)。2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式列入《可用于婴幼儿食品的菌种名单》。
鼠李糖乳酪杆菌 MP108:鼠李糖乳酪杆菌MP108(Lacticaseibacillus rhamnosus?MP108)从健康幼儿肠道分离得到,MP108也是目前全球唯一一株分离自中国宝宝健康肠道的婴幼儿菌株,菌粉性状为白色至微棕色粉末。含有该菌株的产品已在澳大利亚生产并上市,可用于婴幼儿食品。国内外开展的多项婴幼儿临床研究证明,该菌株具有较好的食用安全性。
2021年4月,中华人民共和国国家卫生健康委员会批准鼠李糖乳酪杆菌MP108为新食品原料,批准可用于婴幼儿食品。
罗伊氏粘液乳杆菌 DSM17938:罗伊氏粘液乳杆菌(Limosilactobacillus reuteri DSM17938)DSM17938是罗伊氏乳杆菌ATCC 55730的子代菌株,该菌呈棒状,无芽孢,革兰染色呈阳性。最适合生长温度为30-40℃,适宜PH为5.5-6.2。于1990年由Ivan Casas博士从一位生活在安第斯山脉(位于秘鲁)的妇女母乳中分离出来。《世界胃肠病学组织全球指南(2017更新版)》建议婴儿服用罗伊氏粘液乳杆菌DSM17938作为预防婴儿肠绞痛的措施。
2014年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准罗伊氏粘液乳杆菌DSM17938为新食品原料批准可用于婴幼儿食品。
发酵粘液乳杆菌 CECT5716:发酵粘液乳杆菌CECT5716(Limosilactobacillus fermentum CECT5716) 属于乳杆菌属。该菌种已列入欧盟安全资格认定(QPS)推荐的生物制剂列表中,并列入国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”。2011年发酵乳杆菌列入我国《可用于食品的菌种名单》。发酵粘液乳杆菌CECT5716分离自健康母乳,经接种、发酵培养、浓缩、冷冻干燥制得。该菌种已通过美国食品药品监督管理局的GRAS(一般认为安全的物质)认定,可用于婴幼儿配方粉。
2016年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准发酵粘液乳杆菌CECT5716列入《可用于婴幼儿食品的菌种名单》批准可用于婴幼儿食品。
短双歧杆菌 M-16V:短双歧杆菌M-16V(Bifidobacterium breve M-16V)属于双歧杆菌属,由森永公司研发的专利菌株。该菌种已列入欧盟安全资格认定(QPS)推荐的生物制剂列表中,并列入国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”。2011年短双歧杆菌列入我国《可用于食品的菌种名单》。该菌种已通过美国食品药品监督管理局的GRAS(一般认为安全的物质)认定,可用于婴幼儿配方粉。
2016年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准短双歧杆菌M-16V列入《可用于婴幼儿食品的菌种名单,批准可用于婴幼儿食品。
瑞士乳杆菌 R0052:瑞士乳杆菌R0052(Lactobacillus helveticus R0052)是从乳制品中分离得到,是加拿大拉曼公司专利菌株。瑞士乳杆菌R0052已通过美国食品药品管理局认证为一般认为安全(GRAS)物质。含有这种菌株的产品已在加拿大、波兰、澳大利亚被批准用于婴幼儿。国内外开展的多项婴幼儿临床研究证明,该种菌株具有较好的食用安全性,且耐受性良好。
2020年6月,中华人民共和国国家卫生健康委员会批准瑞士乳杆菌R0052为新食品原料,批准可用于婴幼儿食品。
长双歧杆菌婴儿亚种 R0033:长双歧杆菌婴儿亚种R0033(Bifidobacterium longum subsp. infantis R0033)是从婴儿肠道分离得到,是加拿大拉曼公司专利菌株。长双歧杆菌婴儿亚种R0033已通过美国食品药品管理局认证为一般认为安全(GRAS)物质。含有这种菌株的产品已在加拿大、波兰、澳大利亚被批准用于婴幼儿。国内外开展的多项婴幼儿临床研究证明,该种菌株具有较好的食用安全性,且耐受性良好。
2020年6月,中华人民共和国国家卫生健康委员会批准长双歧杆菌婴儿亚种R003为新食品原料,批准可用于婴幼儿食品。
两歧双歧杆菌 R0071:两歧双歧杆菌R0071(Bifidobacterium bifidum R0071)是从成人肠道分离得到,是加拿大拉曼公司专利菌株。两歧双歧杆菌R0071已通过美国食品药品管理局认证为一般认为安全(GRAS)物质。含有这种菌株的产品已在加拿大、波兰、澳大利亚被批准用于婴幼儿。国内外开展的多项婴幼儿临床研究证明,该种菌株具有较好的食用安全性,且耐受性良好。
2020年6月,中华人民共和国国家卫生健康委员会批准两歧双歧杆菌R0071为新食品原料,批准可用于婴幼儿食品。
长双歧杆菌长亚种 BB536:长双歧杆菌长亚种BB536(Bifidobacterium longum subsp. longum BB536),长双歧杆菌长亚种(原名称为“长双歧杆菌”)已被列入我国《可用于食品的菌种名单》,也已列入欧洲食品安全局资格认定(QPS)名单的推荐生物制剂列表以及国际乳品联合会公报(Bulletin?of?the?IDF?455/2012)的“在发酵食品中有技术必要性的微生物品种目录”。长双歧杆菌长亚种BB536(Bifidobacteriumlongumsubsp.?longumBB536)从健康婴儿肠道中分离得到,该菌株已在美国、日本被批准用于婴幼儿食品。国内外开展的多项婴幼儿临床研究证明,该菌株具有较好的食用安全性。
2022年5月13日卫健委批准长双歧杆菌长亚种BB536为可用于婴幼儿食品的菌种的新食品原料。
参考文献:
1. Lai, H., Li, Y., He, Y., Chen, F., Mi, B., Li, J., ... & Liu, X. (2023). Effects of dietary fibers or probiotics on functional constipation symptoms and roles of gut microbiota: a double-blinded randomized placebo trial. Gut Microbes, 15(1), 2197837.
2. Forsg?rd, R. A., Rode, J., Lobenius-Palmér, K., Kamm, A., Patil, S., Tacken, M. G., ... & Brummer, R. J. (2023). Limosilactobacillus reuteri DSM 17938 supplementation and SARS-CoV-2 specific antibody response in healthy adults: a randomized, triple-blinded, placebo-controlled trial. Gut microbes, 15(1), 2229938.
3. Takeda, T., Asaoka, D., Nojiri, S., Yanagisawa, N., Nishizaki, Y., Osada, T., ... & Sato, N. (2023). Usefulness of Bifidobacterium longum BB536 in elderly individuals with chronic constipation: A randomized controlled trial. The American Journal of Gastroenterology, 118(3), 561.
致谢
特别感谢以下企业对《2023益生菌行业白皮书》的大力支持!
来源:食品伙伴网食品研发创新服务中心,《2023益生菌行业白皮书》作者:陈嘉莉 暨南大学副研究员。
提醒:文章仅供参考,如有不当,欢迎留言指正和交流。且读者不应该在缺乏具体的专业建议的情况下,擅自根据文章内容采取行动,因此导致的损失,本运营方不负责。如文章涉及侵权或不愿我平台发布,请联系处理。










